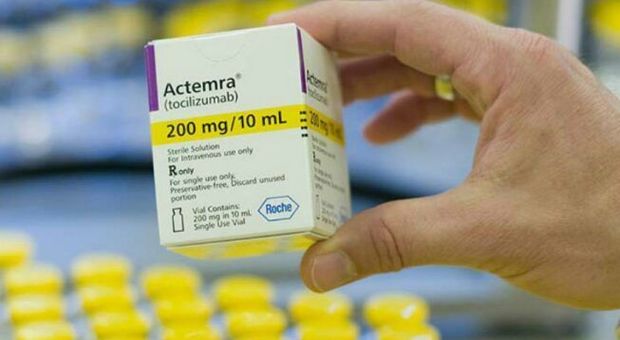
Ad oggi in Puglia il farmaco Tocilizumab della società Roche, somministrato sui pazienti più gravi contagiati dal coronavirus, è in sperimentazione su 11 pazienti e, in base ai protocolli concordati con gli infettivologi, potrebbe essere esteso su altri ammalati. Lo ha comunicato ieri il direttore del dipartimento regionale Salute, Vito Montanaro, ai sindacati durante una video-conferenza. In Puglia l'ok definitivo al Tocilizumab è arrivato nei giorni scorsi dalla giunta regionale che ha approvato l'utilizzo del Roactemra, a base del principio attivo Tocilizumab, fornito dalla ditta farmaceutica Roche. La Regione ha demandato alla commissione tecnica regionale Farmaci la definizione e l'approvazione di un protocollo scientifico per il corretto impiego off-label (cioè nella pratica clinica e fuori dal normale utilizzo) del farmaco Tocilizumab nei pazienti affetti da polmonite interstiziale da Covid-19, con l'individuazione dei criteri di inclusione/esclusione al trattamento e delle misure emergenziali da adottarsi da parte dei Centri individuati che si occupando di gestire gli ammalati.
LEGGI ANCHE: Puglia, 120 nuovi i nuovi contagi: i casi salgono a 906. Trend di crescita stabile
Intanto il presidente dell'Ordine dei medici di Bari, Filippo Anelli, a capo anche della Federazione degli Ordini dei medici italiani, ha rivolto alle Regioni e all'Istituto Superiore della Sanità due richieste. La prima: saturimetri per la gestione domiciliare dei pazienti contagiati dal coronavirus, la seconda: distribuzione dei farmaci antivirali usati contro l'Hiv per prevenire le polmoniti. «Attraverso il saturimetro - chiarisce Anelli - il paziente, grazie anche una consulenza a distanza del medico, può essere tenuto sotto osservazione controllando l'evolversi della malattia. Mentre per quanto riguarda i farmaci antivirali usati contro l'Hiv ormai ci sono evidenze scientifiche e diverse pubblicazioni, anche fatte in Lombardia, che ci dicono che l'uso di questi farmaci, anche a domicilio, in alcuni casi specifici può aiutare a ridurre preventivamente il numero di polmoniti». Le richieste di Anelli puntano ad evitare una eccessiva ospedalizzazione, favorendo l'assistenza domiciliare dei casi positivi ma non in condizioni critiche.
Nel frattempo Pasquale Frega, amministratore delegato del gruppo farmaceutico svizzero Novartis in Italia, in un'intervista al Corriere della Sera ha aperto a una possibile donazione di 130 milioni di dosi di idrossiclorochina. «Un semplice antimalarico - ha spiegato - utilizzato anche per alcune malattie autoimmuni tra cui il lupus eritematoso sistemico e l'artrite reumatoide negli adulti. Ma si comportò assai bene già ai tempi della Sars». Tuttu questo sarà possibile «se la Fda statunitense e l'Agenzia europea per i medicinali ci daranno l'ok».
C'è poi l'Agenzia italiana del farmaco (Aifa) che «procede sulla sperimentazione del medicinale Avigan». Ad annunciarlo ieri il ministro della Salute Roberto Speranza. Il direttore generale di Aifa, Nicola Magrini, ha detto il ministro, «mi ha comunicato che la riunione del Comitato Tecnico-Scientifico, dopo una prima analisi sui dati disponibili relativi ad Avigan, sta sviluppando un programma di sperimentazione e ricerca per valutare l'impatto del farmaco nelle fasi iniziali della malattia». Su questo fronte si registra la richiesta del Veneto. Un video sul web girato da un italiano mostra un farmaco antinfluenzale usato in Giappone contro il nuovo coronavirus che avrebbe ottenuto effetti se somministrato ai primissimi sintomi. Si tratta del Favipiravir (nome commerciale Avigan) un antivirale autorizzato in Giappone dal marzo 2014 per il trattamento di forme di influenza causate da virus influenzali nuovi o riemergenti e il suo utilizzo è limitato ai casi in cui gli altri antivirali sono inefficaci. La Regione Veneto lo vuole. Il governatore, Luca Zaia ha annunciato che «verrà sperimentato anche in Veneto. Spero che da domani (oggi, ndr) si possa partire», dice. L'Agenzia italiana del farmaco (Aifa) ha risposto che avvierà la valutazione ma precisa: «Il medicinale non è autorizzato né in Europa, né negli Usa. Non ci sono prove di efficacia».
© RIPRODUZIONE RISERVATA
Il farmaco per curare l'artrite in sperimentazione su 11 pugliesi
3 Minuti di Lettura
Martedì 24 Marzo 2020, 10:05 - Ultimo aggiornamento: 12:15
© RIPRODUZIONE RISERVATA
